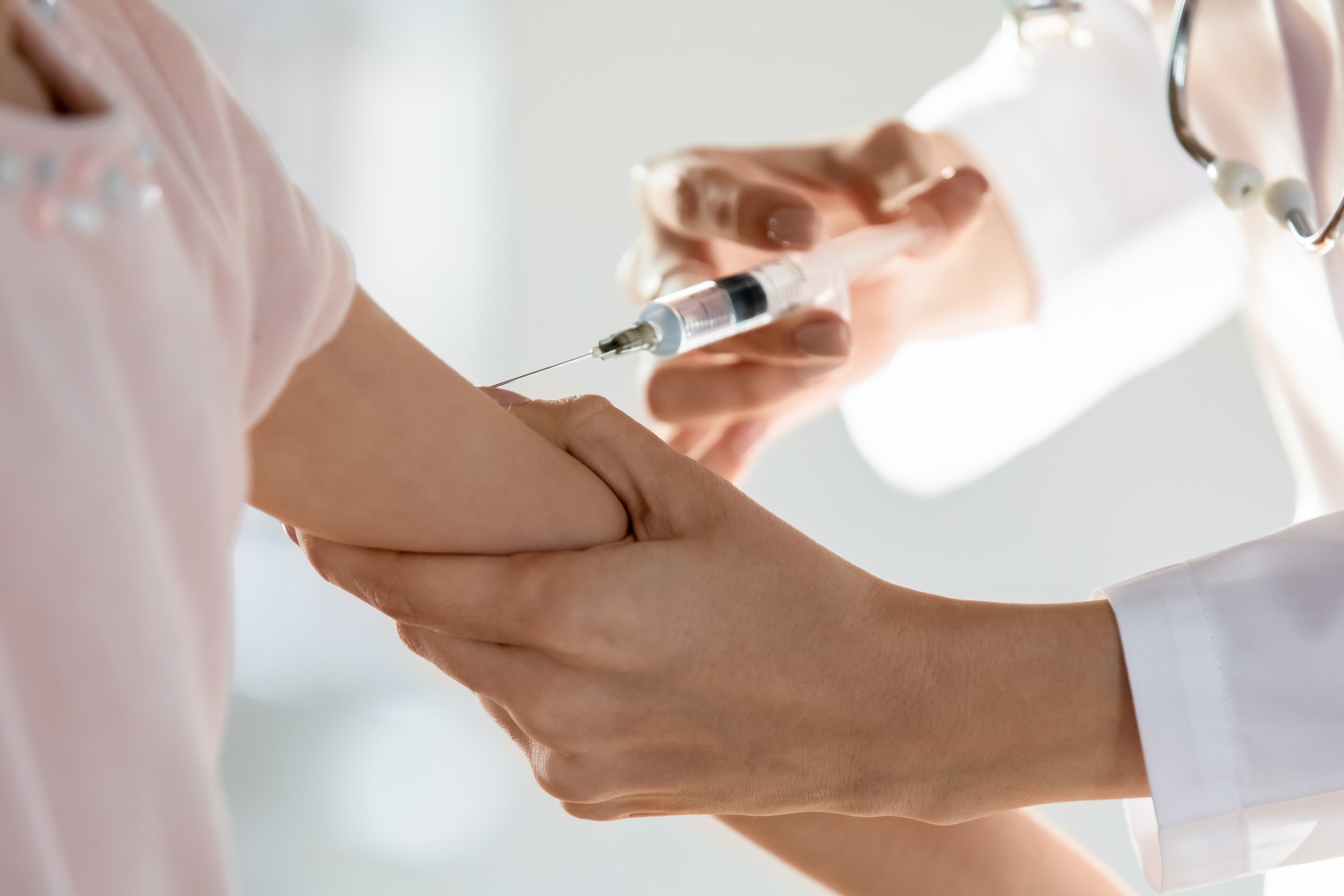
Pełnomocnik podmiotu odpowiedzialnego dla produktu leczniczego Corhydron, kilka miesięcy temu przekazał Głównemu Inspektorowi Farmaceutycznemu informację o uzyskanym wyniku poza specyfikacją jakościową (OOS) w badaniu stabilności dla parametru zawartość wolnego hydrokortyzonu. Chodziło konkretnie o lek w dawce 25, w postaci proszku i rozpuszczalnika do sporządzania roztworu do wstrzykiwań lub do infuzji.
W zgłoszeniu wskazano m.in., iż otrzymane przekroczenie jest nieznaczne, jednak przewidywany jest jego wzrost do końca terminu ważności przedmiotowego produktu. Tymczasem zgodnie z Obwieszczeniem Ministra Zdrowia, produkt jest na wykazie produktów leczniczych wchodzących w skład zestawów przeciwwstrząsowych, ratujących życie.
- Czytaj również: Seria leku Corhydron wstrzymana w obrocie
W związku z uzasadnionym podejrzeniem wystąpienia wady jakościowej, GIF już 21 maja wydał decyzję, którą wstrzymał obrót tym lekiem. Natomiast po przeprowadzeniu postępowania wyjaśniającego, GIF uznał, iż stwierdzona wada stanowi przesłankę do wycofania wskazanej serii leku.
Stąd też 18 września Główny Inspektor Farmaceutyczny wydał decyzję wycofującą z obrotu lek Corhydron 25. Decyzja dotyczy już wcześniej wstrzymanej serii 110021 (termin ważności: 09.2024).
Źródło: ŁW/GIF